|
Agentes Trombolíticos De maneira global, todos os agentes trombolíticos disponíveis reduzem a mortalidade do infarto agudo do miocárdio (IAM) com supra de ST em cerca 30%, ou seja, taxas em torno de 7% a 10% nos grandes ensaios. Nas revisőes de bancos de dados provenientes de comunidades, a mortalidade absoluta tem sido um pouco maior, em torno de 12% a 14%, refletindo melhor a prática clínica. Com base no estudo Gusto-1, o maior ensaio sobre trombolíticos no IAM já realizado, o ativador do plasminogęnio tecidual parece produzir maior benefício global que a estreptoquinase, associando-se a uma reduçăo absoluta da mortalidade de 1% (6,3% vs. 7,3%), o que equivale a uma reduçăo relativa de 15%. Devido ao preço do ativador do plasminogęnio tecidual recombinante (tPA) ser excessivamente maior, a estreptoquinase (SK) deve ser a droga trombolítica de eleiçăo em nosso meio. |
Autores Fernando Oswaldo Dias Rangel - Doutorando de Cardiologia da Universidade Federal do Rio de Janeiro (UFRJ); Presidente do Departamento de Emergęncia e Terapia Intensiva da Sociedade de Cardiologia do Estado do Rio de Janeiro; Médico da Unidade Coronariana do Hospital Pró-Cardíaco; Médico do CTI de pós-operatório do Instituto Nacional de Cardiologia de Laranjeiras. Roberto Esporcatte - Professor Assistente de Cardiologia da Faculdade de Cięncias Médicas da Universidade do Estado do Rio de Janeiro (FCM/Uerj); Coordenador Médico da Unidade Coronariana do Hospital Pró-Cardíaco. |
A clássica indicaçăo para o tratamento trombolítico do IAM é a presença de quadro clínico compatível com isquemia miocárdica aguda refratária ao uso de nitrato sublingual, em associaçăo a alteraçőes eletrocardiográficas (ECG) com supradesnível de segmento ST > 0,1mV em duas ou mais derivaçőes contíguas ou padrăo de bloqueio de ramo recente. O Quadro resume as principais contra-indicaçőes absolutas e relativas ao uso dos agentes trombolíticos referendadas pela Sociedade Brasileira de Cardiologia.
A SK é constituída por uma cadeia polipeptídica única cuja ligaçăo ao plasminogęnio forma um complexo ativo capaz de clivar pontes peptídicas de outras moléculas de plasminogęnio, levando ŕ ativaçăo da plasmina. A dose recomendada é de 1.500.000 unidades administradas em infusăo por 60 minutos. A recomendaçăo de năo-utilizaçăo rotineira de heparina como terapia coadjuvante da trombólise com SK é ainda bastante controversa. No estudo AMI-SK, com quase 500 pacientes, a enoxiparina como terapia coadjuvante foi superior ao placebo, determinando melhor resoluçăo de ST, maior taxa de fluxo Timi-3 (58,7% vs. 70,3%, p = 0,01) ao final de cinco a dez dias e sugerindo menor incidęncia de óbito, infarto ou angina em 30 dias (13,4% vs. 21%).
Outros problemas da SK săo relacionados ŕ sua antigenicidade, propiciando imunossensibilizaçăo e reaçőes alérgicas e recomendando que seja evitada sua readministraçăo no período entre cinco dias e dois anos após uma primeira exposiçăo. A hipotensăo arterial ocorre especialmente com maior velocidade de infusăo (> 500 unidades/kg/min) e pode ser controlada com reposiçăo de cristalóides, interrupçăo ou reduçăo da velocidade de infusăo, ou mesmo com associaçăo de aminas vasoativas como a dopamina. Sangramento é a complicaçăo mais comum, com pequenas hemorragias nos sítios de punçăo em 3% a 4% dos pacientes.
Grandes sangramentos săo menos comuns, e o risco de hemorragia intracraniana é < 1%, elevando-se a 1,6% nos pacientes acima de 70 anos.
O tPA apresenta grande fibrinoespecificidade e, quando ligado ŕ fibrina, aumenta ainda mais sua afinidade pelo plasminogęnio. Outra importante propriedade do tPA é a sua curta meia-vida (tręs a quatro minutos), o que impőe prolongada e complexa administraçăo: 15mg em bolo + 0,75mg/kg (máximo = 50mg) em 30 minutos + 0,5mg/kg (máximo = 35mg) em 60 minutos. Diferentemente da SK, o tPA necessita da administraçăo concomitante de heparina năo-fracionada venosa (que deve ser mantida por pelo menos 24-48 horas) para manter a patęncia vascular e prevenir a reoclusăo, o que representa uma dificuldade a mais. A heparinizaçăo deve ser implementada com ajuste de doses baseado no peso, com ataque de 60U/kg (máximo = 4.000U), seguida de infusăo de 12U/kg/h (iniciar com máximo = 1.000U/h), objetivando tempo de tromboplastina parcial ativado entre 50 e 70 segundos. Embora ainda năo incorporada nas recomendaçőes das principais sociedades de cardiologia, a substituiçăo da heparina năo-fracionada pelas heparinas de baixo peso molecular surge como prática e promissora opçăo terapęutica. No estudo Hart-2, a taxa de patęncia vascular (Timi-2 ou 3) foi maior com enoxiparina do que com heparina năo fracionada (80,1% vs. 75,1%), com menor incidęncia de reoclusăo (5,9% vs. 9,8%). A principal complicaçăo com o uso de tPA é o sangramento, e, em pacientes acima de 70 anos, a incidęncia de acidente vascular encefálico é maior do que com a SK (2,6% vs. 1,6%).

Peso < 70kg, pressăo arterial > 170/95mmHg e
heparinizaçăo agressiva săo outros fatores associados ŕ
maior incidęncia de hemorragia cerebral.
Estes agentes trombolíticos já plenamente incorporados
ao arsenal terapęutico ainda apresentam importantes
limitaçőes, como a falha em obter patęncia
coronariana em 15% a 20% dos pacientes, 10% a 15%
de reoclusăo e o risco de hemorragia intracraniana.
Entre os novos agentes trombolíticos desenvolvidos para
suplantar estas limitaçőes, as drogas obtidas por manipulaçőes
da molécula nativa do tPA, também denominadas
ativadores de plasminogęnio de terceira geraçăo,
onde se destacam o r-PA (ou reteplase), o n-PA
(ou lanoteplase) e o TNK-tPA (ou tenecteplase), săo
as mais amplamente avaliadas em ensaios clínicos.
Outros agentes em estudo săo a estafiloquinase
recombinante e o ativador do plasminogęnio obtido
de uma espécie de morcego hematófago (bat PA). Estes
agentes tęm em comum prolongada meia-vida, o
que possibilita administraçăo em bolo. Tręs deles
(TNK-tPA, estafiloquinase e bat PA) apresentam elevada
fibrinoespecificidade, com conseqüente mínima
degradaçăo de fibrinogęnio, e teoricamente todos seriam
mais potentes na lise do trombo intracoronariano.
Recente revisăo de 38 ensaios envolvendo estes
novos agentes concluiu que o rPA e o TNK-tPA săo
semelhantes ao tPA em termos de eficácia e segurança
(Figura). Embora no estudo InTime-II on-PA apresentasse
a mesma eficácia que o tPA em relaçăo ŕ mortalidade,
a taxa de hemorragia intracraniana foi significativamente
maior (1,12% vs. 0,64%), o que impediu
a sua comercializaçăo. Em contraponto ŕ vantagem da
administraçăo em bolo, todos estes mutantes do tPA
necessitam de heparinizaçăo plena por 24-48 horas.
Entre os novos agentes, apenas o tenecteplase foi recentemente lançado no Brasil, com preço semelhante
ao do tPA.
Os benefícios da terapia trombolítica ou da
angioplastia primária independem da idade, do sexo e
da maioria das características basais. Entretanto os
pacientes que mais se beneficiam com as estratégias de
reperfusăo săo aqueles tratados mais precocemente, os
idosos, aqueles com IAM de parede anterior, ou com
outros aspectos de alto risco.
Terapia combinada de
Embora o ácido acetilsalicílico promova inequívoca
reduçăo da mortalidade por IAM, sua açăo
antiplaquetária é relativamente fraca, pois decorre da
inibiçăo apenas da via do tromboxane A2. Os antagonistas
da glicoproteína IIb/IIIa săo potentes agentes
antiplaquetários que bloqueiam a via final comum da
agregaçăo e adesăo plaquetária. Em face das crescentes
evidęncias de que grande parte do mecanismo
fisiopatológico responsável pelo freqüente insucesso da
trombólise está relacionada ŕ ativaçăo plaquetária, diversos
estudos com a combinaçăo de dose reduzida de
trombolíticos e GP IIb/IIIa tęm sido desenvolvidos.
trombolítico + antagonistas
da GPIIb/IIIa
O estudo Timi-14, um dos mais importantes estudos-
piloto nesta linha de investigaçăo, avaliou o uso
concomitante do abciximab com vários esquemas de
tPA ou SK. Ao final de 90 minutos, as taxas de fluxo
Timi-3 foram de 32% para abciximab isolado, um valor
comparável ŕ SK isolada em outros estudos; 34% a
46% para SK + abciximab; e 61% a 76% para tPA
(meia dose) + abciximab, em comparaçăo com 57%
para tPA (dose plena) isolado. Estes resultados promissores
năo foram confirmados em grandes ensaios.
No estudo Gusto-5, com mais de 16.500 pacientes, o
esquema rPA (meia dose) + abciximab, quando comparado
com rPA (dose padrăo), năo produziu diferença
de mortalidade de 30 dias (5,6% vs. 5,9%). Houve
benefício moderado com a terapia da combinaçăo em
relaçăo ŕ incidęncia de reinfarto năo-fatal (2,3% vs.
3,5%), isquemia recorrente (11,3% vs. 12,8%), necessidade
de revascularizaçăo e outras complicaçőes
năo-fatais do infarto. Năo houve aumento das taxas
de hemorragia intracraniana, mas a combinaçăo aumentou
o risco de outros sangramentos.
O estudo Assent-3 incluiu 6.095 pacientes com
IAM e comparou tręs esquemas: tenecteplase (dose
plena) + enoxiparina, tenecteplase (meia dose) +
heparina năo-fracionada + abciximab, e tenecteplase
(dose plena) + heparina năo-fracionada. Os objetivos
primários (mortalidade em 30 dias, reinfarto ou
isquemia refratária) foram significativamente menores
nos 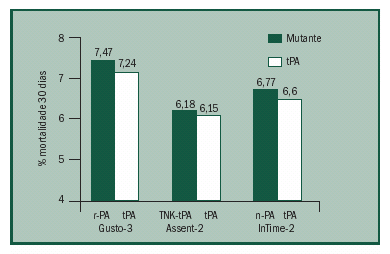 grupos abciximab e enoxiparina em relaçăo ao
grupo heparina năo-fracionada, e equivalentes entre
si: 11,1% (abciximab), 11,4% (enoxiparina) e 15,4%
(heparina năo-fracionada). O mesmo comportamento
foi observado em relaçăo ŕ segurança. Estratégia
semelhante foi avaliada no estudo Entire-Timi-23,
onde 483 pacientes foram tratados de acordo com
quatro esquemas: dose plena de TNK-tPA (com
heparina năo-fracionada ou enoxiparina) ou meia dose
de TNK-tPA + abciximab (com heparina năofracionada
ou enoxiparina). Os resultados sugerem que
a enoxiparina está associada a taxas de fluxo Timi-3 semelhantes
ŕ heparina năo-fracionada na fase inicial da
trombólise, com vantagens em relaçăo aos eventos isquęmicos
ao final de 30 dias, e semelhante risco
hemorrágico. Apesar da pequena casuística, vale ressaltar
que a associaçăo TNK-tPA (dose plena) + enoxiparina
apresentou a menor taxa de eventos isquęmicos (4,4%),
quando comparado com terapia combinada TNK-tPA
(meia dose) + abciximab, tanto com enoxiparina (5,5%)
como com heparina năo-fracionada (6,5%).
grupos abciximab e enoxiparina em relaçăo ao
grupo heparina năo-fracionada, e equivalentes entre
si: 11,1% (abciximab), 11,4% (enoxiparina) e 15,4%
(heparina năo-fracionada). O mesmo comportamento
foi observado em relaçăo ŕ segurança. Estratégia
semelhante foi avaliada no estudo Entire-Timi-23,
onde 483 pacientes foram tratados de acordo com
quatro esquemas: dose plena de TNK-tPA (com
heparina năo-fracionada ou enoxiparina) ou meia dose
de TNK-tPA + abciximab (com heparina năofracionada
ou enoxiparina). Os resultados sugerem que
a enoxiparina está associada a taxas de fluxo Timi-3 semelhantes
ŕ heparina năo-fracionada na fase inicial da
trombólise, com vantagens em relaçăo aos eventos isquęmicos
ao final de 30 dias, e semelhante risco
hemorrágico. Apesar da pequena casuística, vale ressaltar
que a associaçăo TNK-tPA (dose plena) + enoxiparina
apresentou a menor taxa de eventos isquęmicos (4,4%),
quando comparado com terapia combinada TNK-tPA
(meia dose) + abciximab, tanto com enoxiparina (5,5%)
como com heparina năo-fracionada (6,5%).
Estes resultados reafirmam a segurança da enoxiparina
com o tPA e seus mutantes, o que, pela facilidade e custo-
efetividade, parece constituir estratégia atrativa e mais
adequada do que a associaçăo de abciximab a trombolítico.
Em breve tempo, novos ensaios já em curso devem definir
a melhor combinaçăo de trombolíticos e antitrombóticos
no tratamento do IAM.
Em metanálise de seis ensaios e mais de 6.400 pacientes,
a trombólise pré-hospitalar reduziu em quase
uma hora o tempo para início do tratamento (162min
± 16min vs. 104min ± 7min), contribuindo para diminuir
a mortalidade em 17%. No recém-publicado
estudo ER-Timi-19, o tempo médio entre a chegada
ao atendimento de emergęncia e o início da trombólise
com rPA foi reduzido de 63min para 31min, quando
comparadas as abordagens pré-hospitalar e hospitalar.
A mortalidade hospitalar foi de 4,7%, com 1% de hemorragia
intracraniana.
A trombólise pré-hospitalar foi comparada com
a angioplastia primária no estudo Captim, sendo observada
diferença năo-significativa nos objetivos
compostos de mortalidade global, reinfarto ou acidente
vascular encefálico em favor da angioplastia
(8,2% vs. 6,2%).
É importante lembrar que a trombólise pode ser
efetiva mesmo em pacientes com mais de 12 horas de
evoluçăo, principalmente na presença de sintomas e
alteraçőes eletrocardiográficas compatíveis com
isquemia em curso. Os benefícios da trombólise tardia
estăo provavelmente relacionados ŕ patęncia
vascular (hipótese da artéria aberta), com melhor cicatrizaçăo
ventricular, menor expansăo da área de infarto
e maior estabilidade elétrica.
Mais recentemente, o estudo dinamarquęs
Danami-2 demonstrou que a estratégia de transferęncia
dos pacientes para realizar angioplastia primária
reduziu em 40% o risco relativo de óbito, reinfarto ou
acidente vascular encefálico, quando comparada com
a trombólise hospitalar, desde que năo houvesse retardo
maior que tręs horas.
Trombólise em pacientes de
Entre os pacientes de maior atençăo pela alta mortalidade
por IAM destacam-se os subgrupos com tempo
de evoluçăo > 4 horas, localizaçăo anterior, idade >
65 anos, sexo feminino, supradesnível de ST em mais
de seis derivaçőes, bloqueio de ramo adquirido, infarto
prévio, pressăo arterial < 100mmHg, freqüęncia cardíaca
> 100bpm, diabetes melito, insuficięncia cardíaca e choque
cardiogęnico.
alto risco
Trombólise no idoso (classe I se < 75
Com o progressivo envelhecimento da populaçăo,
é cada vez maior o número de pacientes idosos que
apresentam IAM. Independente do tratamento, os
idosos tęm alta mortalidade, e muitos apresentam comorbidades
que podem contra-indicar a terapia
trombolítica.
Sexo feminino
Choque cardiogęnico
Seleçăo do agente trombolítico
anos; classe IIa se 75 anos)
Estudos pioneiros como Gissi-1 e Isis-2 demonstraram
que a mortalidade em pacientes tratados com
SK foi tręs vezes maior nos pacientes > 75 anos, como
seria esperado. A mortalidade foi reduzida em termos
absolutos em 3,9% (25% vs. 29% com placebo), benefício
50% maior que aquele constatado em pacientes
mais jovens (10,7% vs. 8,3%).
No levantamento feito pelo grupo Fibrinolytic Therapy
Trialists´ (FTT), a terapia trombolítica reduziu de forma
significativa a mortalidade para pacientes entre 65 e 74
anos (13,5% vs. 16,1% com placebo, p < 0,00001), mas
năo em pacientes 75 anos (24,3% vs. 25,3%). Em nova
análise deste estudo direcionada para idosos > 75 anos e
considerados elegíveis para trombólise de acordo com os
critérios atuais (elevaçăo de ST ou bloqueio de ramo com
até 12 horas de evoluçăo), a mortalidade ao final de 35
dias foi significativamente reduzida (29,4% vs. 26%,
p = 0,03). Esta reduçăo absoluta de 34 vidas salvas em
mil pacientes tratados é semelhante ŕ observada na faixa
de 65 a 74 anos (40 vidas salvas em mil) e maior do que
em pacientes < 55 anos (16 vidas por mil).
Em contraste com os benefícios da trombólise no
idoso observados nos ensaios clínicos, outros relatos năo
detectaram benefícios. Estudo retrospectivo de um banco
de dados americano (Medicare) com 7.864 pacientes
com idades entre 65 e 86 anos identificou que aqueles
com > 75 anos submetidos ŕ trombólise apresentaram
mortalidade 38% maior ao final de 35 dias, em especial
no sexo feminino. Outro estudo com 37.983 pacientes
65 anos e com IAM năo identificou benefício ao final
de 30 dias, mesmo após correçăo para dados
demográficos, fatores clínicos e intervençőes. Neste
mesmo estudo, o subgrupo tratado com angioplastia
primária apresentou mortalidade 21% menor, mas, ao
final de um ano, as duas estratégias foram benéficas,
com vantagem para o grupo tratado com intervençăo
(reduçăo de mortalidade de 29% vs. 16%).
Apesar do inquestionável benefício da trombólise
para o idoso, sua utilizaçăo é bastante limitada, tanto
na faixa entre 65 e 75 anos (19% de utilizaçăo) como
acima de 75 anos (7,4%), em contraste com o emprego
em metade dos pacientes com menos de 65 anos.
Vários săo os motivos para explicar estas baixas taxas
de utilizaçăo, além da preocupaçăo com sangramentos.
Mais freqüentemente os idosos săo atendidos além das
seis horas do início dos sintomas, e os achados eletrocardiográficos
săo menos diagnósticos de IAM. Os sintomas
de infarto săo menos típicos e a presença de comorbidades
pode contra-indicar o uso de trombolíticos.
De maneira equivocada, o infarto do idoso muitas vezes
é considerado de menor risco.
Em um estudo retrospectivo, a taxa de hemorragia
intracraniana pós-trombólise em pacientes 65
anos foi de 1,43%, observando-se relaçăo direta com
os seguintes preditores independentes: idade 75 anos,
sexo feminino, raça negra, acidente vascular
encefálico prévio, pressăo arterial 160mmHg, uso
de tPA, anticoagulaçăo excessiva (INR 4) e baixo
peso ( 65kg para mulheres e 80kg para homens).
As recomendaçőes atuais săo de que a idade
năo deva impedir a trombólise, classificando-a
como IIa em pacientes > 75 anos.
No estudo Gusto-I, as mulheres apresentaram
maior mortalidade em 30 dias (11,3% vs. 5,5%), diferença
que cai para 15% após ajustes para características
basais, especialmente idade.
No estudo Gusto-I, nos pacientes que năo apresentavam
choque cardiogęnico, o tPA determinou reduçăo
de mortalidade e da taxa de desenvolvimento
de choque, quando comparado com SK. Entretanto,
nos pacientes com choque houve tendęncia năo-significativa
para menor mortalidade com SK. No estudo
Gusto-III, os pacientes com choque cardiogęnico melhoraram
com tPA, mas năo se beneficiaram com rPA.
Năo há dados randomizados demonstrando a eficácia
e a segurança do balăo de contrapulsaçăo intraaórtica
e trombólise no choque cardiogęnico pós-IAM,
mas há sugestőes de eficácia segundo observaçőes dos
estudos Shock e Gusto-1. Assim, a presença de choque
cardiogęnico deve ser vista como fator limitante
da eficácia, e năo como contra-indicaçăo ao uso de
trombolíticos. Neste contexto, o implante da
contrapulsaçăo intra-aórtica deve ser feito cuidadosamente
por profissionais experientes, sem que se retarde
o início da trombólise.
Tanto para pacientes jovens como para idosos que
se apresentam com evidęncia de isquemia miocárdica
aguda, a questăo central é se o paciente é candidato ŕ
trombólise. Se indicada a trombólise, a seleçăo do agente
poderá ser feita com dados oriundos do estudo
Gusto-1, onde 12% e 4% dos pacientes tinham mais
de 75 e 80 anos, respectivamente. Na faixa etária acima
de 75 anos, o tPA em regime acelerado de administraçăo
determinou reduçăo năo-significativa da
mortalidade (19% vs. 21% com SK), mas com expressiva
maior incidęncia de hemorragia intracraniana
(2,1% vs. 1,2%). Em pacientes > 85 anos houve tendęncia
a menor mortalidade com SK (29,4% vs. 30%
com tPA), mas os dados săo muito limitados.
Marcadores de reperfusăo
A qualidade do fluxo coronariano obtida com a
trombólise depende de vários fatores, como a hemodinâmica
(pressăo de perfusăo coronariana, freqüęncia
cardíaca, drenagem venosa), anatomia local (tamanho
e tônus vasculares, localizaçăo, gravidade, extensăo
e geometria da lesăo), quantidade de trombo residual
(tempo para reperfusăo, retrombose, ativaçăo plaquetária
e atividade da trombina) e fatores celulares (funçăo
endotelial, expressăo de moléculas de adesăo,
interaçőes imunológicas e integridade microvascular). A patęncia vascular (fluxo Timi 2 ou 3) pode ser obtida
em 60% a 75% dos pacientes, mas apenas a
reperfusăo ideal ou completa (Timi 3) se traduz em
real reduçăo da mortalidade (3,7% vs. 7% com fluxo
Timi 2). Os pacientes com fluxo Timi 3 também se
caracterizam por menores picos de marcadores de
necrose miocárdica, menos anormalidades de contraçăo
segmentar e menor depressăo da fraçăo de ejeçăo. Os benefícios da reperfusăo plena se estendem a longo
prazo, observando-se menor mortalidade ao final de
dois anos (7,9% vs. 15,7%, fluxo Timi 0, 1 ou 2).
pós-trombólise
Apesar de importante, a detecçăo clínica da
reperfusăo năo pode ser feita de maneira totalmente
confiável na maioria dos pacientes. Por diversos motivos,
o desaparecimento da dor torácica năo pode ser
utilizado como indicativo da eficácia terapęutica. O
comportamento dos marcadores de necrose miocárdica
pode ser útil na identificaçăo da reperfusăo. A
reperfusăo obtida nas seis horas iniciais de evoluçăo
do IAM determina alteraçőes da cinética de liberaçăo
dos marcadores, reduzindo o tempo entre o início do
infarto e o pico de CK, assim como um aumento na
magnitude do pico de CK em relaçăo ao tamanho do
infarto. Isto é mais evidente quando a reperfusăo ocorre
nas primeiras quatro horas. Mais recentemente, foi
descrito que relaçőes entre os níveis séricos aos 60 minutos
após o início da trombólise e basais de mioglobina
4, de CK-MB 3,3 e de troponina I 2 forneceram
probabilidades de Timi II ou III de 90%, 88%
e 87%, respectivamente.
As arritmias de reperfusăo podem oferecer pequena
contribuiçăo na análise da eficácia da trombólise,
pois as mais freqüentemente observadas, como a
taquicardia ventricular e a fibrilaçăo ventricular, também
o săo em pacientes năo-submetidos ou malsucedidos com a terapia trombolítica. Uma arritmia que
tem sido correlacionada com a restauraçăo da patęncia
vascular é o ritmo idioventricular acelerado, freqüentemente
denominado taquicardia ventricular lenta.
Com freqüęncia entre 60bpm e 125bpm, a maioria
dos episódios é de curta duraçăo, terminando abruptamente,
alentecer gradualmente antes do término ou
ser suprimida pela aceleraçăo do ritmo de base. Habitualmente
năo há necessidade de nenhum tratamento
antiarrítmico, pois năo há evidęncias de que possa induzir
taquicardia ou fibrilaçăo ventricular. Se houver
repercussăo clínica (rara) com distúrbio hemodinâmico
ou angina, recomenda-se aceleraçăo da freqüęncia
de base com atropina ou marca-passo atrial.
A regressăo ou resoluçăo da elevaçăo do segmento ST após
a terapia trombolítica é considerada um marcador de
reperfusăo e de valor prognóstico, permitindo identificar
potenciais candidatos ŕ angioplastia de resgate. Ao final de
tręs horas, a resoluçăo completa do ST ( 70% de resoluçăo),
parcial (30% a 70%) ou ausente (< 30%),
correlacionou-se com taxas de mortalidade ao final de cinco
semanas de 2,5%, 4,3% e 17,5% (p < 0,0001), respectivamente.
A regressăo de ST em tręs horas foi o preditor
mais potente de mortalidade e, quando possível, a análise
mais precoce (em 60-90 minutos) pode orientar e antecipar
a decisăo acerca da intervençăo hemodinâmica. A rápida
resoluçăo de ST também se correlaciona com o achado
de recanalizaçăo precoce com adequada perfusăo
miocárdica e melhor contratilidade segmentar. Por outro
lado, a permanęncia de infradesnível de ST em derivaçőes
năo-relacionadas ao infarto ou oscilaçőes recorrentes (elevaçăo
ou depressăo) de ST após a resoluçăo inicial do ST
identificam pacientes de alto risco para eventos adversos. A presença de ondas Q patológicas ou inversăo de onda T
no ECG de admissăo está associada com pior resposta ŕ
trombólise, perfusăo miocárdica inadequada e alteraçőes
de contratilidade segmentar, enquanto que o năo-desenvolvimento
de ondas Q pressupőe menor extensăo e intensidade
de disfunçăo ventricular e melhor perspectiva de
recuperaçăo funcional.
Referęncias Bibliográficas
1. II DIRETRIZES DA SBC PARA O TRATAMENTO DO IAM.
Arq Bras Cardiol, v. 74, suplemento II, p. 1, 2000.
2. DiMARCO, J. Results from late-breaking clinical trials sessions
at ACC 2001. J Am Coll Cardiol, v. 38, p. 595, 2001.
3. ROSS, A. M. et al. Randomized comparison of enoxaparin, a
low-molecular-weight heparin, with unfractioned heparin
adjunctive to recombinant tissue plasminogen activator
thrombolysis and aspirin: second trial of heparin and aspirin
reperfusion therapy (Hart II). Circulation, v. 104, p. 648, 2001.
4. LLEVADOT, J.; GIUGLIANO, R. P.; ANTMAN, E. M. Bolus
fibrinolytic therapy in acute myocardial infarction. JAMA, v. 286,
p. 442, 2001.
5. THE ASSESSMENT OF THE SAFETY AND EFFICACY OF
A NEW THROMBOLYTIC REGIMEN (ASSENT)-3
INVESTIGATORS. Efficacy and safety of tenecteplase in
combination with enoxaparin, abciximab, or unfractionated
heparin: the Assent-3 randomised trial in acute myocardial
infarction. Lancet, v. 358, p. 605, 2001.
6. ANTMAN, E. M. et al. Enoxiparin as adjunctive antithrombin
therapy for ST-elevation myocardial infarction: results of the Entire-
Thrombolysis in Myocardial Infarction (Timi) trial. Circulation, v.
105, p. 1642, 2002.
7. MORRISON, L. J.; VERBEEK, P. R.; McDONALD, A. C.
Mortality and prehospital thrombolysis for acute myocardial
infarction: a metaanalysis. JAMA, v. 283, p. 2686, 2000.
8. MORROW, D. A. et al. Evaluation of the time saved by
prehospital initiation of reteplase for ST-elevation myocardial
infarction: results of the Early Retavase-Thrombolysis In Myocardial
Infarction (ER-Timi)19 trial. J Am Coll Cardiol, v. 40, p. 71, 2002.
9. WILLIAMS, E. S. Results from late-breaking clinical trial sessions
at the American College of Cardiology 51st annual scientific session.
J Am Coll Cardiol, v. 40, p. 1, 2002.
10. WONG, C-K.; WHITE, H. D. Medical treatment for acute
coronary syndromes. Curr Opin Cardiol, v. 15, p. 441, 2000.
11. THIEMANN, D. R. et al. Lack of benefit for intravenous
thrombolysis in patients with myocardial infarction who are older
than 75 years. Circulation, v. 101, p. 2239, 2000.
12. BERGER, A. K. et al. Thrombolytic therapy in older patients.
J Am Coll Cardiol, v. 36, p. 366, 2000.
13. GURWITZ, J. H. et al. Recent age-related trends in the use of
thrombolytic therapy in patients who have had acute myocardial
infarction. Ann Intern Med, v. 124, p. 283, 1996.
14. BRASS, L. M. et al. Intracranial hemorrhage associated with
thrombolytic therapy for elederly patients with acute myocardial
infarction: results from the Cooperative Cardiovascular Project.
Stroke, v. 31, p. 1802, 2000.
15. PAUL, S. D. et al. Do gender-based differences in presentation
and management influence predictors of hospitalization costs and
length of stay after an acute myocardial infarction. Am J Cardiol, v.
76, p. 1122, 1995.
16. WHITE, H. D. et al. For the Gusto-1 Investigators. Age and
outcome with contemporary thrombolytic therapy: results from the
Gusto-1 trial. Circulation, v. 94, p. 1826, 1996.
17. SANBORN, T. A. et al. Impact of thrombolysis, intra-aortic
balloon pump counterpulsation, and their combination in
cardiogenic shock complicating acute myocardial infarction: a report
from the shock trial registry. Should we emergently revacularize
occluded coronaries for cardiogenic shock? J Am Coll Cardiol, v.
36, n. 3, suppl. A, p. 1123, 2000.
18. ANDERSON, R. D. et al. Use of intra-aortic balloon counterpulsation
in patients presenting with cardiogenic shock: observations from the Gusto-
1 study. J Am Coll Cardiol, v. 30, p. 708, 1997.
19. GIBSON, C. M. et al. Determinants of coronary blood flow
after thrombolytic administration. Timi Study Group.
Thrombolysis in Myocardial Infarction. J Am Coll Cardiol, v. 34,
p. 1403, 1999.
20. ANDERSON, J. L.; KARAGOUNIS, L. A.; CALIFF, R. M.
Meta-analysis of five reported studies on the relation of early coronary
patency grades with mortality and outcomes after acute myocardial
infarction. Am J Cardiol, v. 78, p. 1, 1996.
21. TANASIJEVIC, M. J. et al. Myoglobin, creatine-kinase-MB
and cardiac troponin-I 60 minute ratios predict infarct-related
artery patency after thrombolysis for acute myocardial infarction:
results from the Thrombolysis in Myocardial Infarction Study
(Timi) 10B. J Am Coll Cardiol, v. 34, p. 739, 1999.
22. SCHRODER, R. et al. For the Injetct Trial Group. Extent of
early ST segment elevation resolution. A strong predictor of outcome
in patients with acute myocardial infarction and a sensitive measure
to compare thrombolytic regimens. A substudy of the International
Joint Efficacy Comparison of Thrombolytics (Inject) Trial. J Am Coll
Cardiol, v. 26, p. 1657, 1996.
23. DE LEMOS, J. A.; BRAUNWALD, E. ST segment
resolution as a tool for assessing the efficacy of a reperfusion
therapy. J Am Coll Cardiol, v. 38, p. 1283, 2001.