| As bases atuais do tratamento da insuficięncia cardíaca (IC) foram estabelecidas em 1987 com o estudo Consensus, quando foi comprovado o benefício do inibidor da enzima conversora da angiotensina (Ieca) na melhora clínica, na reduçăo da mortalidade e na progressăo da insuficięncia cardíaca. Portanto, há 15 anos o tripé terapęutico tem sido a associaçăo de digital, Ieca e diurético. O racional desta terapęutica baseia-se na progressăo da insuficięncia cardíaca sistólica, onde a piora progressiva da doença se deve a um processo contínuo de remodelagem ventricular no decorrer dos anos, associado a uma queda progressiva da funçăo ventricular e reduçăo da sobrevida (Figura 1). A fisiopatologia deste processo tem como fator determinante a desmodulaçăo do sistema neuro-humoral-citocinas, que inicialmente é ativado com o objetivo de estimular alteraçőes cardiovasculares e no conteúdo de sódio e água para estabelecer sustentaçăo da hemodinâmica e da funçăo cardíaca. A estimulaçăo deste sistema acaba cronicamente promovendo mais disfunçăo e remodelagem ventricular e progressăo da insuficięncia cardíaca. Portanto a modulaçăo neuro-humoral-citocinas hoje é a base fisiológica do racional da terapęutica da IC. O entendimento inicial da ativaçăo deste sistema sugeria uma ativaçăo escalonada e progressiva (Figura 2a), onde quanto maior a gravidade ou progressăo da IC, mais sistemas seriam ativados com o objetivo de estabelecer sustentaçăo cardiovascular. Na verdade, a ativaçăo destes sistemas é simultânea (Figura 2b), com um mesmo mediador ativando vários sistemas ao mesmo tempo, com um tropismo inicial maior para o sistema simpático, ao mesmo tempo em que promove a ativaçăo do sistema renina-angiotensina-aldosterona (SRAA), endotelina, vasopressina, citocinas e dos sistemas moduladores, bradicina, prostaglandinas e fator peptídeo natriurético atrial. Ŕ medida que ocorre progressăo da disfunçăo cardíaca, temos uma ativaçăo cada vez mais intensa, com uma interaçăo cada vez maior de seus mediadores, com um sistema potencializando as açőes do outro. Portanto a terapęutica da IC tem como objetivo a modulaçăo do modelo de ativaçăo fisiológica múltipla, com uma atuaçăo terapęutica de controle de múltiplas vias. |
Autores Charles Maddy - Professor Associado da Faculdade de Medicina da Universidade de Săo Paulo (USP); Diretor de Unidade do Incor. Marcelo Westerlund Montera - Professor de pós-gaduaçăo em Cardiologia da Santa Casa do Rio de Janeiro; Professor de Cardiologia da Universidade Gama Filho (UGF); Doutorando em Cardiologia pela USP; Médico do Hospital Pró-Cardíaco. |
Seguindo este racional, o primeiro modelo terapęutico, como já citado anteriormente, foi o de controle de uma via, através do bloqueio (Figura 3) da enzima de conversăo da angiotensina I para angiotensina II, que se mostrou eficaz nos resultados do estudo Consensus e de todos os outros que o sucederam utilizando o mesmo princípio. Mas, dentro deste modelo do bloqueio de uma via, por vezes poderia haver uma atuaçăo mais eficaz e com menos paraefeitos com medicamentos que agissem de forma mais específica junto aos receptores que medeiam a parte final da cascata de ativaçăo neuro-humoral. Em funçăo deste raciocínio temos o desenvolvimento dos bloqueadores dos receptores AT1, que tęm uma atuaçăo mais distal em uma via. O estudo Elite II năo conseguiu demonstrar o benefício deste racional, onde o losartan năo demonstrou ser superior ao captopril na reduçăo da mortalidade total (- 12%) e da morte súbita (- 20%), sugerindo que um bloqueio mais inespecífico desta via (SRAA) ocasionaria efeitos em outras vias (bradicinina e 1Professor Associado da Faculdade de Medicina da Universidade de Săo Paulo (USP); Diretor de Unidade do Incor. 2Professor de pós-gaduaçăo em Cardiologia da Santa Casa do Rio de Janeiro; Professor de Cardiologia da Universidade Gama Filho (UGF); Doutorando em Cardiologia pela USP; Médico do Hospital Pró-Cardíaco. prostaciclinas), ampliando o benefício de sua atuaçăo. Ainda dentro da avaliaçăo do bloqueio de uma via, tentou- se demonstrar que o bloqueio maximizado poderia trazer benefícios adicionais ao bloqueio de uma única via. Esta hipótese foi testada no estudo Atlas, no qual năo se comprovou benefício adicional no uso de doses elevadas de lisinopril na reduçăo da mortalidade geral e cardiovascular, tendo benefício somente na reduçăo de reinternaçăo hospitalar (Figura 3). Portanto o aumento da posologia na tentativa de ampliar a atuaçăo terapęutica do bloqueio de uma via năo se mostrou eficaz. Desta forma, um bloqueio, năo de uma via, mas, sim, de duas vias, poderia ter uma atuaçăo mais eficaz na modulaçăo do sistema neuro-humoral.
Esta possibilidade foi avaliada no estudo Val-HeFT, com a associaçăo de enalapril com valsartan (bloqueio de duas vias) em comparaçăo com enalapril (bloqueio de uma via). Năo se observou benefício adicional na reduçăo da mortalidade (19,4% vs 19,7%), e, sim, de eventos combinados de mortalidade com eventos combinados de reinternaçăo e piora da IC (28,8% com enalapril vs 32,1% com enalapril + valsartan; p = 0,009). Com a suspeita de que um bloqueio mais amplo ou de múltiplas vias seria mais eficaz e se traduziria em maiores benefícios terapęuticos, o bloqueio de tręs vias, com adiçăo de espirolactona, que ocasiona um bloqueio específico da via da aldosterona, evitando o escape da aldosterona que ocorre em cerca de 27% dos pacientes em uso de Ieca, como demonstrado por Alison, teria mais benefício que o bloqueio de duas vias.
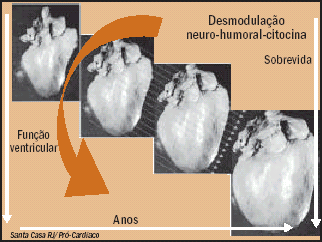 Figura 1. Desmodulaçăo neuro-humoral-citocina e progressăo da remodelagem ventricular com piora prognóstica evolutiva |
Esta possibilidade foi validada pelo estudo Rales, que demonstrou que a adiçăo de espirolactona na terapęutica com IECA, digital e diurético da IC, ocasiona um benefício adicional de reduçăo de risco de mortalidade de 30%.
Sendo assim, o bloqueio de quatro vias poderia ter um benefício ainda maior na melhora clínica e na reduçăo da mortalidade por IC (Figura 3). Esta possibilidade foi testada com o uso do omopatrilato, que tem a propriedade de atuar no bloqueio do SRAA e inibir a açăo da endopeptidase, que é a enzima responsável pela degradaçăo do peptídeo atrial natriurético (PAN).
O PAN tem açăo vasodilatadora e diurética, com efeitos anti-remodelagem e de modulaçăo do SRAA, endotelina e vasopressina, e, portanto, o aumento dos seus níveis séricos através da inibiçăo de sua degradaçăo poderia ter benefícios terapęuticos por ter uma atuaçăo fisiológica múltipla. Inicialmente esta possibilidade foi sugerida no estudo Impress, no qual o omopatrilato apresentou uma taxa de mortalidade combinada com hospitalizaçăo 47% menor que o lisinopril. Como este estudo foi realizado com pequeno número de pacientes, um novo estudo com maior número de pacientes, denominado Overture, teve os seus resultados apresentados este ano no congresso do Colégio Americano de Cardiologia, e năo se demonstraram benefício na associaçăo do omopatrilato com a terapęutica usual para IC na reduçăo da mortalidade (p = 0,3; RR: 0,94), eventos combinados de morte com hospitalizaçăo (p = 0,18; RR: 0,94), morte cardiovascular com hospitalizaçăo cardiovascular (p = 0,02; RR: 0,91) e morte com infarto do miocárdio, hospitalizaçăo e acidente vascular encefálico (p = 0,2; RR: 0,93).
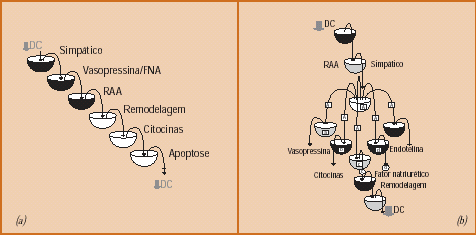 Figura 2a. Modelo de ativaçăo escalonado dos sistemas neurohumorais Figura 2b. Modelo de ativaçăo múltipla neurohumoral |
Na análise dos paraefeitos, a associaçăo de omopatrilato apresentou maior incidęncia de hipotensăo arterial (19,5% vs 11,5%). Estes resultados levantam o questionamento de que o bloqueio de múltiplas vias pode ocasionar a perda de mecanismos fisiológicos necessários para a sustentaçăo cardiovascular e hemodinâmica, em que os benefícios da modulaçăo neuro-humoral seriam suplantados pelo desenvolvimento de paraefeitos, o que vem a sugerir que um bloqueio de múltiplas vias (mais do que tręs vias) pode ocasionar efeitos além dos desejáveis para controle da IC. Ao invés de bloquearmos de forma múltipla a via do peptídeo atrial natriurético, podemos amplificar a atuaçăo de seus efeitos moduladores do sistema neurohumoral através da reposiçăo de um similar sintético do fator natriurético B(FNB) (Figura 3).
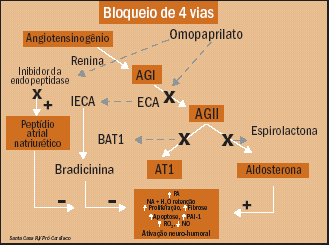 Figura 3. Bloqueio terapęutico múltiplo das vias de ativaçăo humoral |
O neseritide, composto sintético do FNB, foi avaliado em pacientes com IC aguda por via parenteral, em que foi observada uma importante melhora clínica intra-hospitalar, com reduçăo das pressőes de enchimento de forma mais efetiva que a nitroglicerina venosa e reduçăo da readmissăo hospitalar e mortalidade em seis meses, em comparaçăo com a dobutamina. O neseritide apresenta-se como uma nova medicaçăo que poderá vir a ser de grande utilidade para o tratamento das formas agudas de IC.
Observando o racional de que o bloqueio de múltiplas vias poderá ocasionar perda de efeitos desejáveis de sustentaçăo cardiovascular, a utilizaçăo de bloqueadores dos receptores da endotelina associados com a terapęutica usual da IC ocasiona um bloqueio de quatro vias. A utilizaçăo do bosentan, antagonista dos receptores da endotelina, adicionado ŕ terapęutica da IC em pacientes com importante disfunçăo ventricular, foi avaliada no estudo Enable e apresentada este ano no congresso do Colégio Americano de Cardiologia, e os resultados năo demonstraram benefício na reduçăo da mortalidade, mas uma maior tendęncia ŕ retençăo hídrica e hipotensăo arterial no grupo do bosentan. Estes resultados vęm mais uma vez enfatizar os malefícios do bloqueio múltiplo extenso, ultrapassando os benefícios da modulaçăo neuro-humoral. Paralelamente ŕ modulaçăo humoral, temos o controle da atividade neural com a utilizaçăo de betabloqueadores (Figura 4).
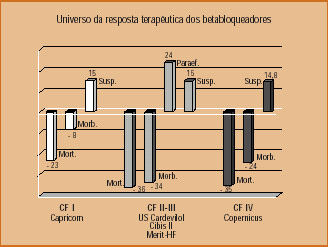 Figura 4. Benefícios terapęuticos com o uso de betabloqueadores na reduçăo da mortalidade e eventos mórbidos nas diferentes fases clínicas de insuficięncia cardíaca e incidęncia de intolerância |
O benefício da utilizaçăo dos betabloqueadores está bem estabelecido nos pacientes com IC classe funcional II e III da New York Heart Association (NYHA), na melhora da sobrevida, da funçăo ventricular e da qualidade de vida. Nos pacientes com classes funcionais I e IV, ainda năo estăo bem estabelecidos o seu benefício terapęutico e a segurança de sua utilizaçăo. O benefício da utilizaçăo do carvedilol em pacientes com classes funcionais I e III-IV de IC foi demonstrado em dois estudos, Capricorn e Copernicus. O estudo Capricorn avaliou pacientes com disfunçăo ventricular pós-infarto do miocárdio clinicamente assintomáticos. Os resultados demonstraram uma reduçăo de 23% de mortalidade cardiovascular (p = 0,031), principalmente por morte súbita (26%), e evento combinado de mortalidade global e infarto do miocárdio năo-fatal (p = 0,002; RR: 0,71). O estudo Copernicus avaliou pacientes com importante disfunçăo ventricular e em classe funcional IIIIV da NYHA e demonstrou um benefício com a utilizaçăo do carvedilol, com uma reduçăo de 35% na mortalidade (p < 0,001) e de 24% nos eventos combinados de internaçăo e morte (p < 0,001). Estes benefícios foram também observados em subgrupos de pacientes com formas mais avançadas de IC na reduçăo da mortalidade anual: 42% nos Universo da resposta terapęutica dos betabloqueadores 15 - 8 - 23 - 36 - 35 - 34 - 24 24 15 14,8 Susp. Susp. Susp. Paraef. Morb. Morb. Morb. Mort. Capricorn Copernicus Mort. CF I US Cardevilol Cibis II Merit-HF CF II-III CF IV Mort. Bloqueio de 4 vias Omopaprilato AGI ECA IECA BAT1 Bradicinina AGII AT1 Aldosterona Angiotensinogęnio Espirolactona Proliferaçăo, Fibrose Apoptose, PAI-1 PA RO2, NO NA + H2O retençăo Ativaçăo neuro-humoral Renina Inibidor da endopeptidase Peptídio atrial natriurético X X X X + + – – Santa Casa RJ/Pró-Cardíaco pacientes com fraçăo de ejeçăo < 20% e com uma internaçăo anual, 36% nos pacientes com fraçăo de ejeçăo < 15% e com tręs internaçőes anuais, e de 50% nos pacientes com insuficięncia cardíaca congestiva que necessitaram fazer uso de inotrópicos e com mais de tręs internaçőes em um ano. Portanto a utilizaçăo dos betabloqueadores no tratamento da IC tem agora o seu benefício e a segurança de sua utilizaçăo comprovados em todas as classes funcionais da IC (Figura 4). Quando se avalia o benefício da utilizaçăo dos betabloqueadores na modulaçăo neuro-humoral através do bloqueio terapęutico múltiplo e da análise de projeçăo de resultados, no estudo SOLVD, nota-se que a adiçăo de betabloqueador ŕ terapęutica com Ieca ocasiona uma reduçăo de 60% na internaçăo anual por IC, em comparaçăo com 30% com o uso de Ieca isolado. Numa mesma análise de projeçăo no estudo Rales, encontramos benefício semelhante com a adiçăo de carvedilol ŕ espirolactona, ocasionando uma reduçăo da mortalidade de 58% comparada a 27% no uso năo-associado da espirolactona. Nas formas avançadas de IC, temos ativaçăo de forma significativa do sistema das citocinas (TNF alfa e interleucinas). Estes componentes de atividade inflamatória exercem um efeito de depressăo da contratilidade miocárdica, promoçăo da fibrose, proliferaçăo do colágeno e ativaçăo da cascata enzimática da apoptose. A atividade do sistema das citocinas é independente e sinérgica com o sistema neuro-humoral. A ativaçăo deste sistema promove a progressăo da IC com piora clínica da remodelagem ventricular e pior prognóstico a longo prazo. O benefício do bloqueio da via da citocina tem sido demonstrado em pequenos estudos com o uso da pentoxifilina associada com digital, Ieca e betabloqueadores. A pentoxifilina tem uma atuaçăo de bloqueio da transcriçăo do RNA do TNF no núcleo do miócito. Os resultados demonstram melhora da classe funcional, fraçăo de ejeçăo do ventrículo esquerdo e reduçăo de eventos mórbidos ao fim de seis meses de acompanhamento. Com o mesmo racional de modulaçăo da via inflamatória, a utilizaçăo de imunoglobulina em formas agudas de IC por miocardite periparto demonstra uma melhora significativa na classe funcional e fraçăo de ejeçăo do ventrículo esquerdo. Resultados semelhantes foram observados na utilizaçăo em cardiomiopatia dilatada com importante disfunçăo ventricular, ao fim de seis meses de acompanhamento. O benefício da associaçăo dos moduladores da via inflamatória com Ieca e betabloqueadores está no sinergismo de atuaçăo destas medicaçőes na modulaçăo inflamatória. O enalapril reduz a produçăo da interleucina 6, e o metoprolol reduz a produçăo das interleucinas 1 e 6 e do TNF alfa. Embora o racional do bloqueio da via inflamatória esteja bem evidente, a utilizaçăo de anticorpos anti-TNF alfa na IC năo apresentou benefício, como demonstrado no estudo Renaissance/Recover, que foi interrompido antes do tempo previsto. Uma nova linha de medicaçőes está em desenvolvimento, sendo o levosimendan o mais recente para utilizaçăo no armamentário terapęutico da IC aguda. Esta droga tem a propriedade de aumentar a afinidade do cálcio ao sítio C da troponina, aumentar a ativaçăo dos canais L de cálcio na membrana citoplasmática e ativar os canais de ATP de potássio. Os benefícios hemodinâmicos demonstrados foram a melhora na contratilidade miocárdica com resultante aumento do volume sistólico do débito cardíaco e reduçăo da resistęncia arterial sistęmica e pulmonar. Comparado com a dobutamina, o levosimendan alcança benefício hemodinâmico em 88% dos pacientes, enquanto que a dobutamina, em 70%. Outra medicaçăo para uso em formas crônicas de IC é o pimobendan, que também tem propriedades sensibilizadoras do cálcio e de reduçăo da ativaçăo da via inflamatória por ocasionar uma reduçăo de 70% na ativaçăo do óxido nítrico sintetase com conseqüente reduçăo do óxido nítrico, que é o mais importante mediador da atividade inflamatória das citocinas. O benefício do bloqueio terapęutico múltiplo neuro-humoral-citocina modificou a história natural da IC, com melhora do prognóstico, a longo prazo, de todas as classes funcionais. A mortalidade ao fim de um ano na classe funcional IV tem sido de 18% a 22%; na classe funcional II-III, 6% a 8%, e na classe funcional I, 2% a 4%. A evoluçăo do racional da terapęutica na IC deve migrar de um modelo de bloqueio múltiplo dos sistemas de sustentaçăo para um modelo que visa ŕ atuaçăo direta nos determinantes de formaçăo de doença, através da bioengenharia e terapia celular, podendo evoluir definitivamente para o controle eficaz da insuficięncia cardíaca.
Referęncias Bibliográficas
1. KATZ, A. Heart Failure. Pathophysiology, molecular biology, and clinical management. Lippincott Williams & Wilkins, 2000.
2. PITT, B.; POOLE-WILSON, P. A.; SEGAL, R. Effect of losartan with captopril on mortality in patients with symptomatic heart failure: rationale, design, and baseline characteristics of patients in the Losartan Heart Failure Survival Study-Elite II. Lancet, v. 355, p. 1582-7, 2000.
3. PACKER, M. et al. Comparative effects of low and high doses of the ACE inhibitor, lisinopril, on morbidity and mortality in chronic heart failure. Circulation, v. 100, p. 2312-8, 1999.
4. COHN, J. et al. Valsartan heart failure trial-Val-HeFT. European J of Heart Failure, v. 3, p. 117-24, 2001.
5. YOUN, J. et al. Vasodilatation in the management of acute CHF. VMAC. Presented at the American College of Cardiology 51st Annual Scientific Session. March 20, 2002.
6. PITT, B. et al. The effect of spirolactone on morbidity and mortality in patients with severe heart failure. N Engl J Med, v. 341, p. 709-17, 1999.
7. ALISON, F. C. et al. Neurohormonal reactivation in heart failure patients on chronic ACE inhibitor therapy: a longitudinal study. European Journal of Heart Failure, v. 1, p. 401-6, 1999.
8. ROULEAU, J. L. et al. Comparison of a vasopeptidase inhibitor, omapatrilato, and lisinopril on exercise tolerance and morbidity in patients with heart failure: Impress randomized trial. Lancet, v. 356, p. 615-20, 2000.
9. PACKER, M. et al. Overture. Presented at the American College of Cardiology 51st Annual Scientific Session. March 20, 2002.
10. PACKER, M. et al. Enable. Presented at the American College of Cardiology 51st Annual Scientific Session. March 20, 2002.
11. PACKER, M. et al. Effect of carvedilol on survival in severe chronic heart failure. Copernicus. N Engl J Med, v. 344, p. 1651-8, 2001.
12. THE CAPRICORN INVESTIGATORS. Effect of carvedilol on outcome after myocardial infarction in patients with left ventricular dysfunction: the Capricorn randomized trial. Lancet, v. 357, p. 1385-9, 2001.
13. SKUDICKY, D. et al. Beneficial effects of pentoxifylline in patients with idiopathic dilated cardiomyopathy treated with angiotensin-converting enzyme inhibitors and carvedilol. Results of a randomized study. Circulation, v. 103, p. 1083-8, 2001.
14. GULLESTAD, L. et al. Effect of high- versus low-dose.
15. Angiotensin converting enzyme inhibition on cytokine levels in chronic heart failure. J Am Coll Cardiol, v. 34, p. 2061-7, 1999.
16. PRABHU, S. D. et al. Adrenergic blockade in developing heart failure effects on myocardial inflammatory cytokines, nitric oxide, and remodeling. Circulation, v. 101, p. 2103-9, 2000.
17. GULLESTAD, L. et al. Immunomodulating therapy with intravenous immunoglobulin in patients with chronic heart failure. Circulation, v. 103, p. 220-5, 2001.
18. BOZKURT, B. et al. Intravenous immune globulin in the therapy of peripartum cardiomyopathy. J Am Coll Cardiol, v. 34, p. 177-80, 1999.
19. IWASAKI, A. et al. Pimobendan inhibits the production of proinflammatory cytokines and gene expression of inducible nitric oxide synthase in a murine model of viral myocarditis. J Am Coll Cardiol, v. 33, p. 1400-7, 1999.
20. BOZKURT et al. Renaissance/Recover. Circulation, v. 103, p. 1044-7, 2001.